椺偊偽変乆偺寣塼偺拞偺僿儌僌儘價儞偲偄偆暔幙偱偼巁慺塣斃傪偮偐偝偳傞嵟傕廳梫側晹暘偼 揝偺嶖懱偲側偭偰偄傑偡丏偩偐傜揝偑晄懌偡傞偲昻寣偵側傞偺偱偡丏 怉暔偺岝崌惉偺嵺偵拞怱揑栶妱傪壥偨偡僋儘儘僼傿儖傕儅僌僱僔僂儉偺嶖懱偱偡丏 偙偺岝崌惉偺偍偐偘偱変乆偼巁慺傪媧偭偰惗偒偰偄傞偺偱偡丏 怴惗帣梡偺暡儈儖僋偺娛傪尒偰傒傞偲丆尨椏偺棑偵偼側傫偲栆撆偲巚傢傟偄偰偄傞棸巁摵偑巊傢傟偰偄傞偙偲偑傢偐傝傑偡丏偮傑傝旝検偺摵偼懱偵偲偭偰昁梫側傕偺側偺偱偡丏 変乆偼晛抜怘傋偰偄傞怘暔偐傜摵傪傎傫偺傢偢偐偱偡偑愛庢偟偰偄傞偺偱偡丏
惗暔偼傎偲傫偳偺僷乕僣偑桳婡暔偐傜偱偒偰偄傑偡丏桳婡暔偡側傢偪C, H, N, O偁偨傝偺尨巕偱偱偒偰偄傞偺偑変乆偺懱偺傎偲傫偳偱偁傝丆柍婡尦慺(摿偵嬥懏尦慺)偼懡偔偼偁傝傑偣傫丏偟偐偟丆嬥懏尦慺偱偟偐偱偒側偄栶妱傕偼偨偟偰偄傞偺偱偡丏椺偊偽崪偺庡惉暘偼僇儖僔僂儉儕儞巁墫傗傾僷僞僀僩乮Ca10(PO4)6(OH)2乯偱偁傝丆僇儖僔僂儉偼変乆偺崪奿偺宍惉偵懡検偵巊傢傟偰偄傑偡丏偙偺僇儖僔僂儉偺傛偆側嬥懏尦慺偲堎側傝丆旝検偱偼偁傝傑偡偑廳梫側摥偒傪偟偰偄傞尦慺傕懡偄偺偱偡丏曣擕傪偺傫偱偄傞愒偪傖傫偼曣擕偺拞偵傗偼傝旝検偺嬥懏僀僆儞偑娷傑傟偰偄傞偺偱 偦傟傪愛庢偱偒傑偡丏暡儈儖僋偩偗偟偐偺傑側偄愒偪傖傫偱傕昁梫尦慺偑愛庢偱偒傞傛偆 摵傗垷墧側偳偺嬥懏尦慺偑暡儈儖僋偵偼壛偊偰偁傞偺偱偡丏偙傟傜偺旝検尦慺偺摥偒偵偼傑偩枹夝柧偺柺傕懡偄偺偱偡偑丆 嵟嬤師戞偵偙傟傜偺廳梫惈偑傑偡傑偡巜揈偝傟傞傛偆偵側偭偰偒傑偟偨丏偙偙偱偼偄偔偮偐偺椺傪尒偰偄偒傑偟傚偆丏
1乯丂嵶朎撪奜偵偍偗傞僫僩儕僂儉偲僇儕僂儉
懡偔偺摦暔偱偼嵶朎撪偱偼僇儕僂儉擹搙偑嵶朎奜傛傝崅偔丆媡偵僫僩儕僂儉擹搙偼嵶朎奜偺曽偑崅偔側偭偰偄傑偡丏傕偟僫僩儕僂儉僀僆儞側偳偑帺桼偵嵶朎偺撪奜傪峴偒棃偱偒傞偺偱偁傟偽丆偄偢傟嵶朎撪奜偱僀僆儞偺擹搙偼摍偟偔側傞偼偢偱偡丏偟偐偟忋偺傛偆偵偦偆偱偼側偄偺偼丆峫偊偰傒傞偲戝曄晄巚媍側尰徾偱偡丏偙傟偼ATP偺僄僱儖僊乕傪棙梡偟偨岻柇側巇慻傒偑偐偐傢偭偰偄傑偡丏椺偊偽偙偺傾僯儊傪嶲峫偵偟偰壓偝偄丏偙傟傜偺僀僆儞偺擹搙偺曄壔偼嵶朎娫偺怣崋揱払偵傕怺偔娭學偟偰偄傞丏
2乯丂僿儌僌儘價儞偲僿儉
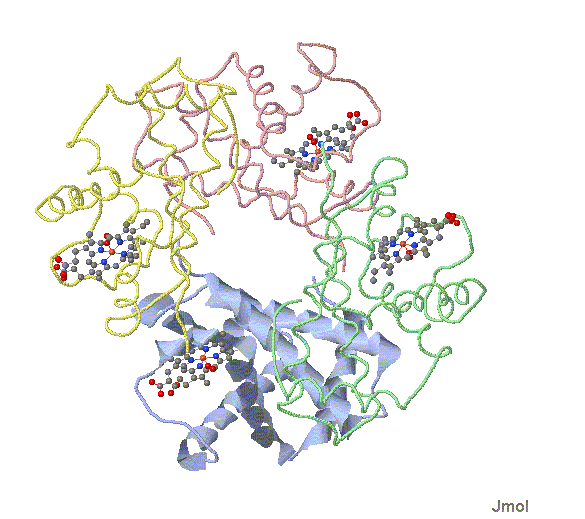
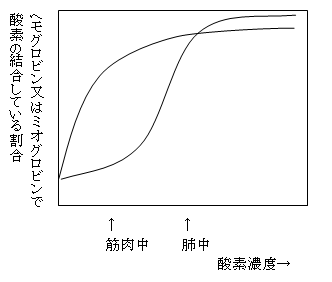
変乆偺寣塼拞偵偼僿儌僌儘價儞偑偁傝傑偡丏僿儌僌儘價儞偼暘巕検64000偺嫄戝側僞儞僷僋幙暘巕偱偁傝丆巁慺傪寣塼拞偱懱偺嬿乆傑偱塣斃偡傞摥偒傪扴偭偰偄偰4偮偺僒僽儐僯僢僩偲屇偽傟傞晹昳偐傜偱偒偰偄傑偡(嵍壓恾)丏偙傟偵懳偟嬝擏拞偵懚嵼偟丆巁慺傪堦師挋憼偡傞摥偒偑偁傞儈僆僌儘價儞偼暘巕検偑栺1枩8000偺僞儞僷僋幙偱偡丏儈僆僌儘價儞偵偼侾偮丆僿儌僌儘價儞偵偼4偮僿儉偲偄偆揝嶖懱偑娷傑傟偰偄傑偡丏僿儉偼億儖僼傿儕儞偲屇偽傟傞娐忬偺桳婡暔偺拞偵揝偑擖偭偨嶖懱偱偁傝丆巁慺暘巕偑寢崌偟傑偡丏嫽枴怺偄偺偼儈僆僌儘價儞偲僿儌僌儘價儞偺巁 偺寢崌惈偱偡丏儈僆僌儘價儞偼巁慺暘埑偑憹偊傞偵廬偭偰塃恾偺傛偆偵巁慺偑寢崌偟偰偄偔丏偮傑傝巁慺暘埑偺忋徃偲嫟偵媫寖偵巁慺偑儈僆僌儘價儞偵寢崌偟偰偄偒傑偡丏偟偐偟丆僿儌僌儘價儞偼丆巁慺暘埑偑掅偄撪偼偁傑傝巁慺偑寢崌偣偢丆偁傞掱搙巁慺暘埑偑崅偔側傞偲媫寖偵巁慺偑寢崌偡傞傛偆偵側傞偲偄偆惈幙偑偁傞偺偱偡丏攛偺拞偲嬝擏拞偺巁慺暘埑傪峫偊傞偲丆僿儌僌儘價儞偑懡検偺巁慺傪塣斃偡傞偺偵桳棙偱偁傞偙偲偑暘偐傞偱偟傚偆丏偙傟偼僿儌僌儘價儞偺撪偺堦偮偺儐僯僢僩偺僿儉偵巁慺偑寢崌偡傞偲懠偺儐僯僢僩偺僿儉偼傛傝巁慺偑寢崌偟傗偡偄傛偆偵峔 偑旝柇偵曄壔偡傞偙偲偵傛偭偰偄傞偺偱偡丏


忋偼僿儌僌儘價儞偺暘巕峔憿偱偡丏儅僂僗偱僪儔僢僌偡傞偲夞揮偡傞偙偲偑偱偒傑偡丏傑偨丆shift僉乕傪墴偟側偑傜儅僂僗傪忋壓偵僪儔僢僌偝偣傟偽僘乕儈儞僌偡傞偙偲偑壜擻偱偡丏偙偺拞偵僿儉暘巕偑偄傞偐偳偆偐扵偟偰傒偰壓偝偄丏
丂側偍丆僀僇側偳偺擃懱摦暔拞偱偼僿儌僔傾僯儞偲屇偽傟傞摵嶖懱偑巁慺塣斃傪巌偭偰偄傑偡丏丂
3乯丂僋儘儘僼傿儖偲岝崌惉
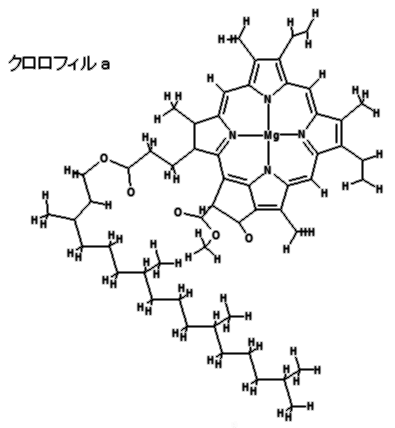
岝崌惉偼偛懚偠偺捠傝丆擇巁壔扽慺偲悈偐傜扽悈壔暔偲巁慺傪嶌傞斀墳偱偡丏偙傟偼旕忢偵暋嶨側斀墳偱偁傝丆岝傪昁梫偲偡傞柧斀墳偲昁梫偲偟側偄埫斀墳傪娷傫偱偄傑偡丏岝崌惉偼懡偔偺暘巕偑娭傢偭偰偄傞斀墳偱偡偑丆拞怱偵側傞偺偼僋儘儘僼傿儖偱偡丏偦偺暘巕偺峔憿偼壓偺偲偍傝偱丆僿儉偲帡偨峔憿偺僐儕儞崪奿傪桳偡傞嶖懱偱偁傝丆拞怱偵儅僌僱僔僂儉傪娷傫偱偄傑偡丏
3乯丂僇儖儃僉僔儁僾僠僟乕僛偲垷墧
垷墧偼懡偔偺峺慺偺摥偒偵娭梌偟偰偄傑偡丏嵟傕弶婜偵偦偺婡峔偑夝柧偝傟偨偺偼媿偺僇儖儃僉僔儁僾僠僟乕僛乮傾儈僲巁偺儁僾僠僪寢崌傪壛悈暘夝偡傞峺慺乯偱偟偨丏偙偺峺慺偼307屄偺傾儈僲巁偑寢崌偟偨僞儞僷僋幙偱偁傝丆侾屄偺垷墧傪娷傫偱偄傑偡丏